汎胃炎④(胃内視鏡/胃カメラ)
胃MALTリンパ腫では、腫瘤形成に乏しく、胃全体にびまん性炎症様変化を呈することがあり、このようなタイプは汎胃炎類似型(pangastritis-like appearance)に分類されます(1)(2)(3)。
内視鏡的には、胃全体の発赤、浮腫、顆粒状変化、白苔付着などを示し(3)(4)、明らかな潰瘍や隆起を欠きH. pylori関連慢性胃炎との鑑別が困難な場合があります(2)(3)。
背景にHelicobacter pylori感染を伴う症例が多く、炎症性変化が前景に立つことが特徴です(2)(5)。
病変が多発・びまん性ではあるものの、限局的な狙撃生検のみでは診断に至らないことがあるため、胃全体からの多点・広範囲生検が診断上重要とされています(7)。
治療は、限局期においてはH. pylori除菌により内視鏡像および病理所見が改善・消失する症例が多いとされています(2)(5)。
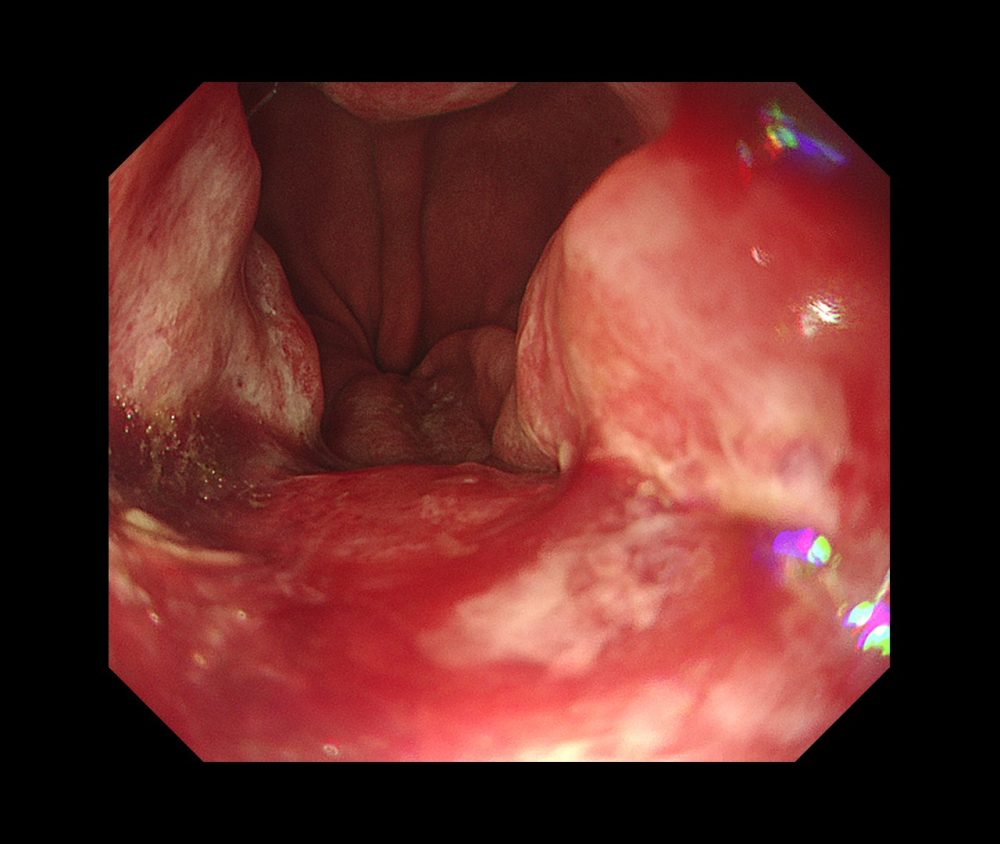
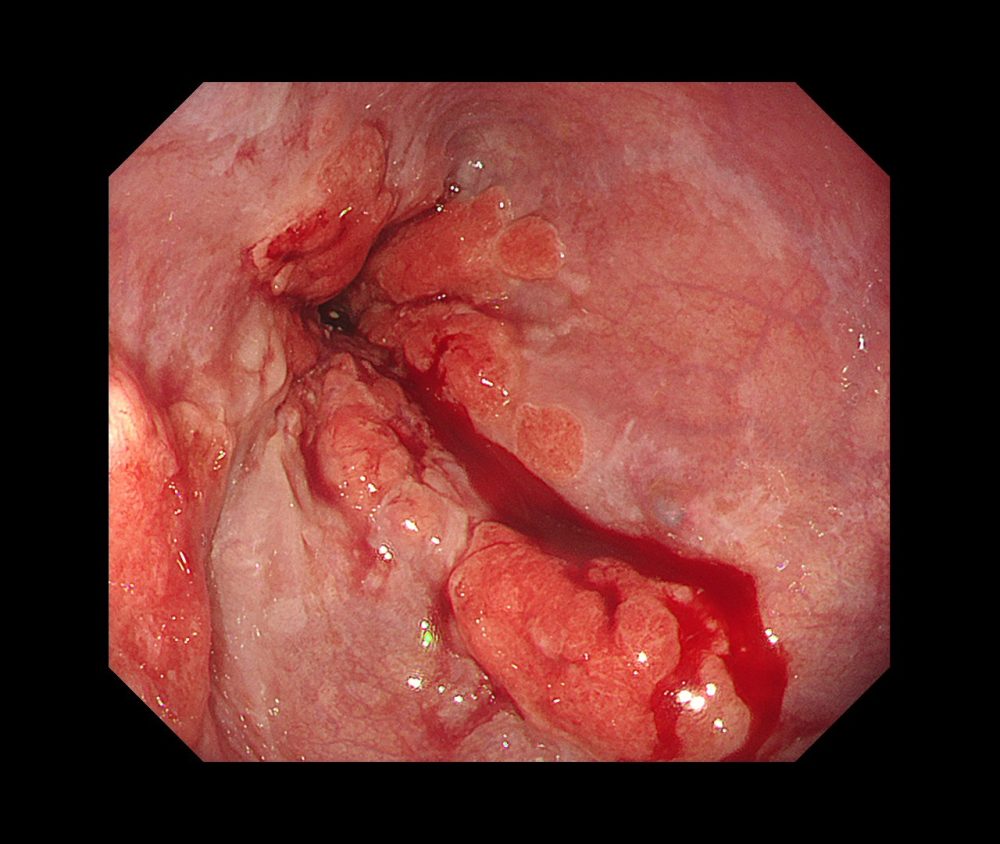
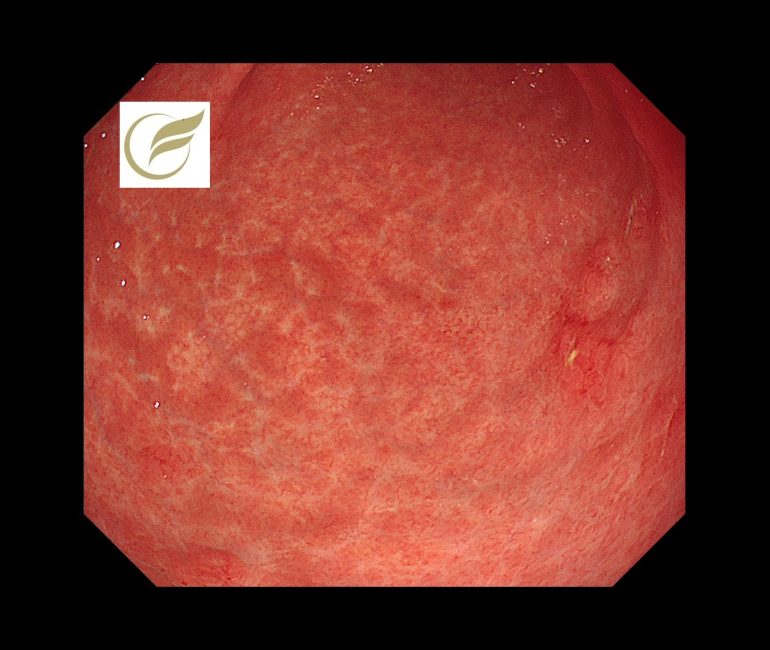
以下は当院で経験された胃MALTです。胃は全体的に萎縮を示し、体部では広範な褪色調粘膜と顆粒状の残存胃底腺粘膜がみられ、胃角部では多発びらんを伴っており、多点生検により胃MALTと診断されました。
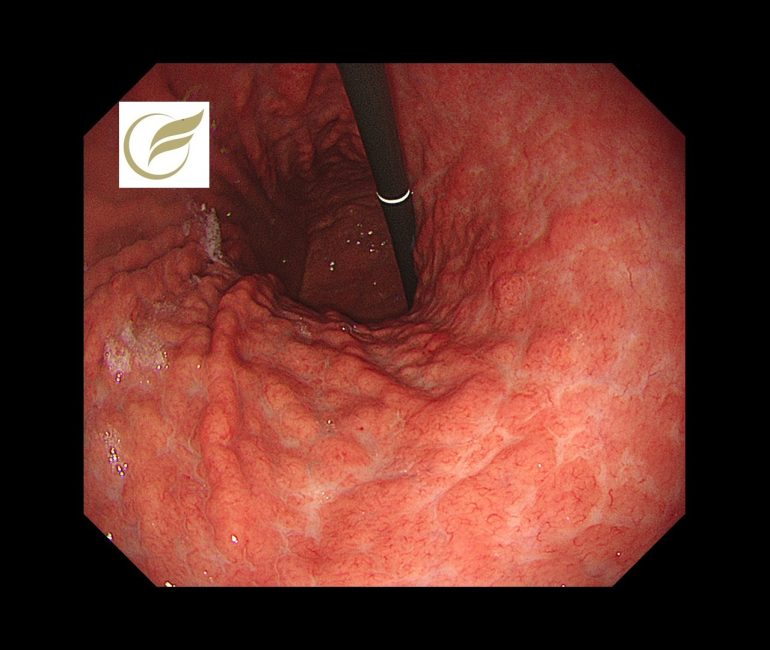
文責 院長 岡田和久
(参考文献)
(1)Isaacson PG, Wright DH. Malignant lymphoma of mucosa-associated lymphoid tissue: a distinctive type of B-cell lymphoma.
Cancer. 1983; 52(8): 1410–1416.
(2)Wotherspoon AC, Ortiz-Hidalgo C, Falzon MR, Isaacson PG. Helicobacter pylori-associated gastritis and primary B-cell gastric lymphoma.
Lancet. 1991; 338(8776): 1175–1176.
(3)Nakamura S, Yao T, Aoyagi K, et al. Helicobacter pylori and primary gastric lymphoma: a histopathologic and immunohistochemical analysis of 237 patients.
Cancer. 1997; 79(1): 3–11.
(4)Zucca E, Roggero E, Bertoni F, Cavalli F. Primary extranodal non-Hodgkin’s lymphomas. Part 1: Gastrointestinal, cutaneous and genitourinary lymphomas.
Ann Oncol. 1997; 8(8): 727–737.
(5)Zullo A, Hassan C, Cristofari F, et al. Effects of Helicobacter pylori eradication on early stage gastric mucosa-associated lymphoid tissue lymphoma.
Clin Gastroenterol Hepatol. 2010; 8(2): 105–110.
(6)Zucca E, Bertoni F. Gastric marginal zone lymphoma of MALT type: ESMO clinical practice guidelines.
Ann Oncol. 2013; 24(Suppl 6): vi144–vi148.
汎胃炎③/好酸球性胃腸炎②(胃内視鏡/胃カメラ)
二次性好酸球性胃腸炎は、特定の原因により消化管に好酸球浸潤を来す状態をいい(1)(2)、原因として、食品(プロテイン・特定食物)、薬剤、寄生虫感染、アレルギー疾患、全身性疾患などが知られています(2)(3)。
一次性については、以下もご参照ください。https://www.jiyugaoka-gc.com/medicalinformation/gastroscope/2317/
症状は腹痛、下痢、嘔吐など非特異的で一次性と区別しがたく(4)、病理学的にも一次性と同様に好酸球浸潤を認めますが、形態的な差は乏しいとされています(5)。
内視鏡所見は非特異的で、発赤、浮腫、顆粒状粘膜、びらん、潰瘍などがみられます(4)(7)(8)。
病変は限局せず、びまん性あるいは多発性に分布することが多く(7)、肉眼的に正常に見える粘膜から好酸球浸潤が検出されることもあります(8)。
また内視鏡像のみで、他疾患あるいは一次・二次とを鑑別することは困難で、外観に関わらず多点生検が重要です(4)(9)。
治療は、原因物質の除去や基礎疾患の治療が基本となり、診断の本質も原因検索とその除外・中止により症状や病理所見が改善するかどうかにあります(1)(6)(10)。
以下の症例は、生検で好酸球浸潤(平均100/HPF以上)が確認され、プロテイン内服による好酸球性胃炎様変化(二次性)疑いとなり、プロテイン中止により速やかに症状(腹痛・嘔吐など)が消失した症例です。前庭部の複数の白色調の細顆粒状~粒状隆起、網目状のひび割れ所見(11)に類似した所見を認めました。
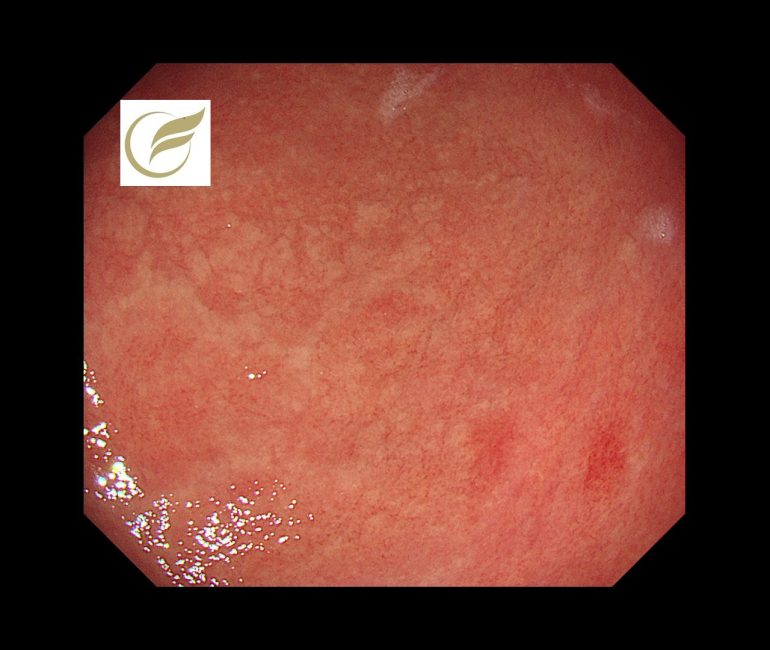
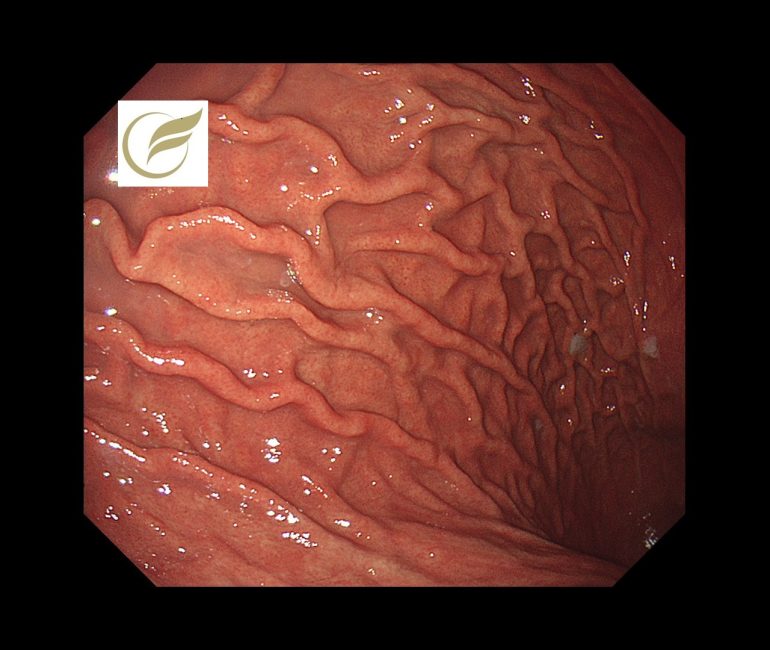
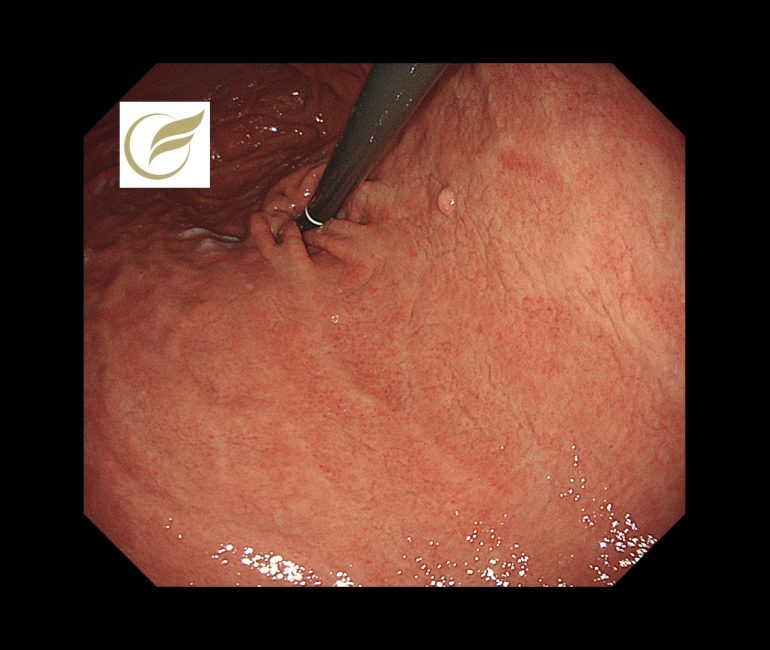
(1)Klein NC, et al. Eosinophilic gastroenteritis. Medicine (Baltimore). 1970;49:299–319.
(2)Rothenberg ME. Eosinophilic gastrointestinal disorders. J Allergy Clin Immunol. 2004;113:11–28.
(3)Lucendo AJ. Eosinophilic diseases of the gastrointestinal tract. Scand J Gastroenterol. 2010;45:1013–1021.
(4)Talley NJ, et al. Eosinophilic gastroenteritis: a clinicopathological study. Gastroenterology. 1990;99:1762–1770.
(5)Dellon ES, et al. Diagnostic criteria for eosinophilic gastrointestinal disorders. J Allergy Clin Immunol. 2013;131:1355–1363.
(6)Pesek RD, et al. Eosinophilic gastrointestinal diseases. Ann Allergy Asthma Immunol. 2014;113:1–9.
(7)Zhang M, et al. Endoscopic features of eosinophilic gastroenteritis. Endoscopy. 2019;51:477–485.
(8)Ingle SB, et al. Eosinophilic gastroenteritis: an unusual type of gastroenteritis. World J Gastroenterol. 2013;19:5061–5066.
(9)Ko HM, et al. Eosinophilic gastritis and enteritis. Arch Pathol Lab Med. 2014;138:1310–1318.
(10)Lucendo AJ, et al. Treatment of eosinophilic gastroenteritis. Curr Opin Gastroenterol. 2017;33:442–447.
(11)Fujiwara Y, et al : Endoscopic findings of gastric lesions in patients with eosinophilic gastrointestinal disorders.Endosc Int Open 8 : E1817―E1825, 2020.
文責 院長 岡田和久
除菌後胃癌(胃内視鏡/胃カメラ)
除菌後胃癌は、Helicobacter pylori 除菌が成功した後に発見される胃癌をいいます(1)(2)。
日本の胃がん死亡者数は徐々に漸減傾向ですが、いまだ年約4万人が罹患し、がん死亡者数の第 3 位を占めています。除菌後に定期的な内視鏡検査を実施しているにも関わらず、進行胃癌で発見される症例もあり、除菌後の早期胃癌の内視鏡診断は難しいとされています。
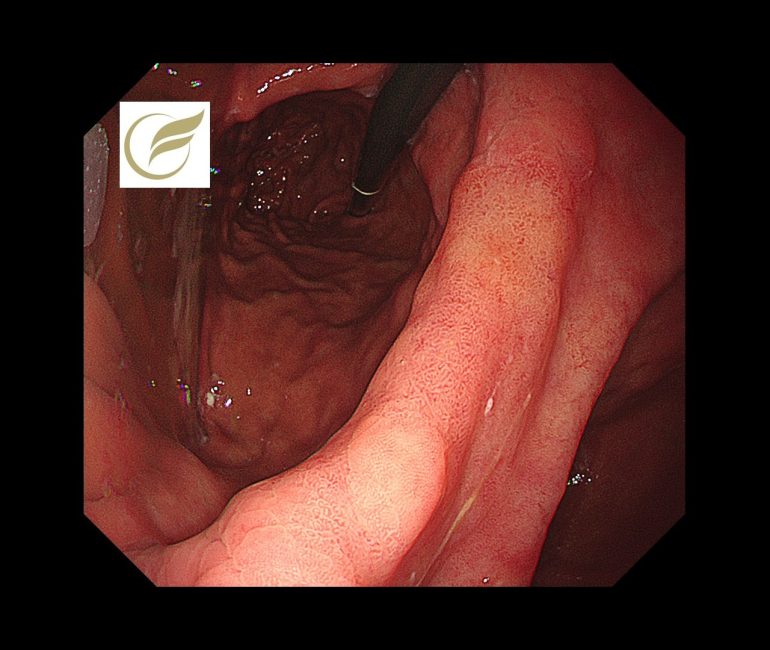
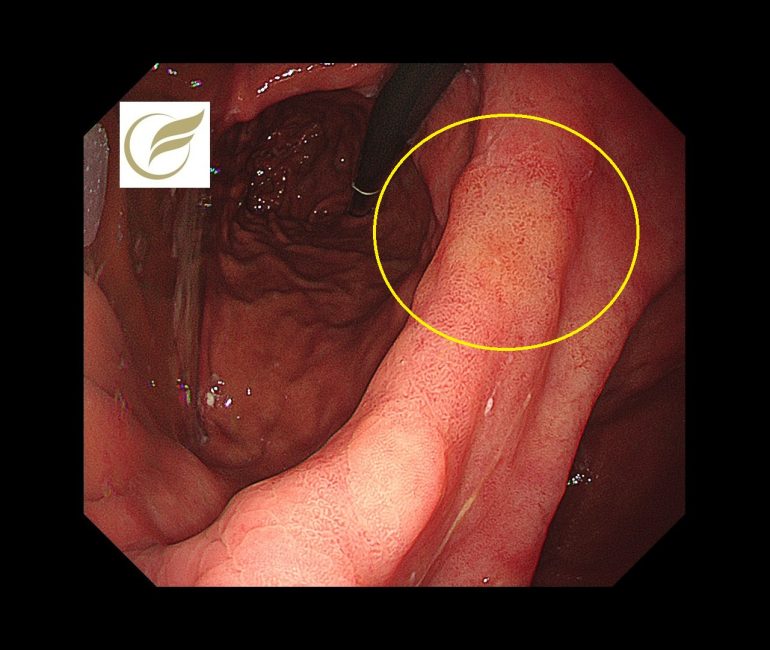
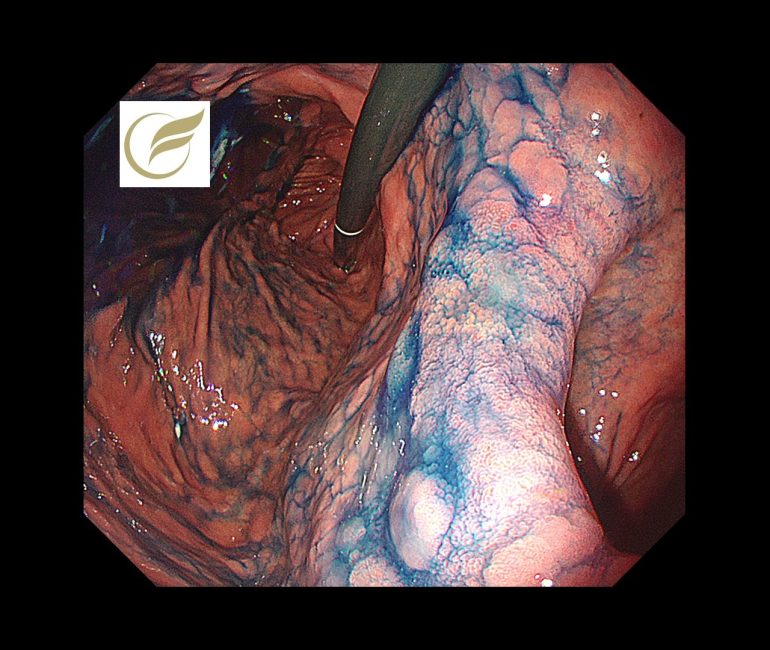
その理由のひとつに、除菌後においては背景胃粘膜の炎症が改善することで、病変と周囲粘膜との色調の差が乏しくなり発見が難しくなることがあるため(1)(4)、ときに病変が周囲粘膜に自然に溶け込むように存在し、病変と正常粘膜の境界が不明瞭となってしまうことがあげられます(4)(5)。さらに肉眼的な形態について、平坦型やごく浅い陥凹型が多く、明らかな隆起を示しにくくなる傾向があり(3)(5)、病変径が小さい上にはっきりとした陥凹を呈することがないため、典型的な悪性所見に乏しい症例も多く経験されます(1)(3)(6)。背景に萎縮や腸上皮化生を伴うことで、粘膜模様が均一化し、病変の認識がさらに難しくなることも、見逃されやすくなる原因である報告されています(4)(5)(7)。最近では、除菌後の背景粘膜が炎症軽減で均質化し病変が周囲に溶け込むような色調となった結果、除菌後胃癌が黄白色〜黄調に見えるようになるという色調・可視性に関する議論もされています(9)。除菌後症例においては、より丁寧な観察が重要となります(1)(2)(10)。
以下の病変は当院で経験された除菌後の早期胃癌(高分化型腺癌)の症例です。黄(白)色調に視認され、典型的な除菌後胃がんの特徴を示していました。
参考文献
(1)Uemura N, Okamoto S, Yamamoto S, et al. Helicobacter pylori infection and the development of gastric cancer. New England Journal of Medicine. 2001; 345(11): 784–789.
(2)Fukase K, Kato M, Kikuchi S, et al. Effect of eradication of Helicobacter pylori on incidence of metachronous gastric carcinoma after endoscopic resection of early gastric cancer: an open-label, randomized controlled trial. The Lancet. 2008; 372(9636): 392–397.
(3)Yamada M, Saito Y, Mori Y, et al. Characteristics of gastric cancer detected after Helicobacter pylori eradication. Gastric Cancer. 2016; 19(2): 468–476.
(4)Shichijo S, Hirata Y. Characteristics and management of gastric cancer after Helicobacter pylori eradication. World Journal of Gastroenterology. 2018; 24(20): 2163–2172.
(5)Kobayashi M, Hashimoto S, Nishikura K, et al. Endoscopic characteristics of gastric cancer after Helicobacter pylori eradication. Digestive Endoscopy. 2013; 25(5): 503–510.
(6)Matsuo T, Ito M, Takata S, et al. Clinicopathological features of early gastric cancer detected after Helicobacter pylori eradication. Digestion. 2012; 85(4): 279–285.
(7)Muto M, Yao K, Kaise M, et al. Magnifying endoscopy with narrow-band imaging for diagnosis of gastric cancer: a prospective multicenter study. Endoscopy. 2009; 41(7): 583–589.
(8)Pimentel-Nunes P, Libânio D, Lage J, et al. Endoscopic diagnosis of gastric lesions after Helicobacter pylori eradication. Endoscopy. 2016; 48(6): 527–536.
(9) Li H, Zhang Z, Wang W, et al. Endoscopic characteristics and high-risk background mucosal factors of early gastric cancer after Helicobacter pylori eradication.
Frontiers in Oncology. 2023; 13:1272187. doi:10.3389/fonc.2023.1272187.
(10)Japanese Gastric Cancer Association. Japanese gastric cancer treatment guidelines 2021 (6th edition). Gastric Cancer. 2023; 26(1): 1–25.
Double pylorus(胃内視鏡/胃カメラ)
-
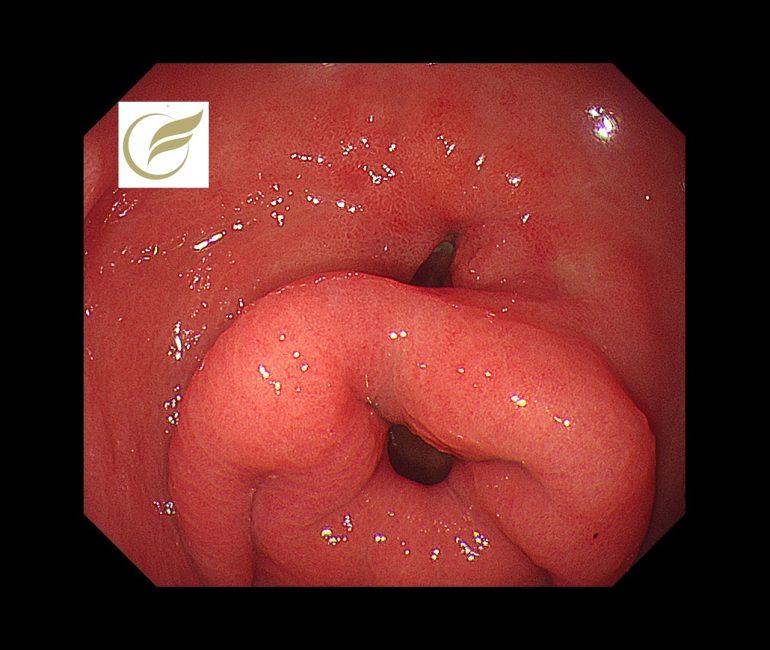
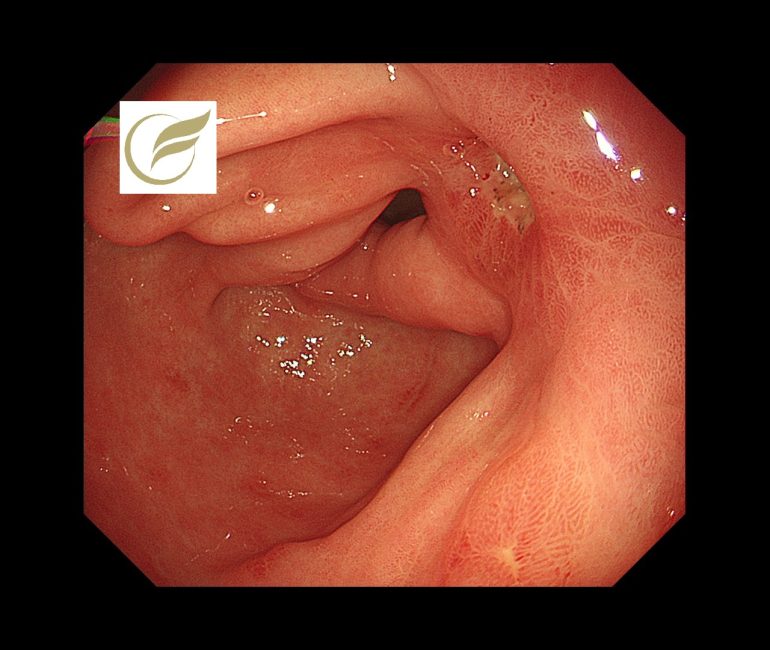
二重幽門は、胃の幽門部から十二指腸球部への副経路が存在するまれな内視鏡所見をいいます。
-
主には胃と十二指腸の間に形成された瘻孔(fistula)により、上部消化管内視鏡検査の中で、0.001% ~ 0.4%という非常に稀な割合で報告されています(1)。
-
先天性と後天性に分類され、先天性は発生期における管腔の異常形成によるもので、通路間の組織が正常で潰瘍病変がないのが特徴とされ、多くは無症状で偶然発見されており、特に治療は不要とされています(2)。
-
後天性は先天性よりも頻度が高く、胃潰瘍や十二指腸潰瘍が進行した結果、胃と十二指腸球部の壁が癒着して瘻孔が形成されるものをいい、NSAIDsやステロイドの使用、Helicobacter pylori(ピロリ菌)感染、糖尿病、慢性呼吸器疾患、SLE、腎不全、ベーチェット病など、潰瘍治癒遅延を引き起こしやすい病態が関連していると報告されています(3、4、5)。
- 後天性も発見時には無症状のことが多く、穿孔・出血などがなければ、病態に応じてピロリ除菌や原因薬剤の中止、酸分泌抑制薬の投与などで経過をみることになります。後天性の自然経過についての後ろ向き追跡調査によれば、酸分泌抑制薬で治療を受けた場合においても瘻孔は大多数(64%)で開存したままで、27%が中隔が消失して正常幽門と癒合し、閉鎖された例はわずか9%だったとされています(3)。
-
内視鏡治療や薬物治療が無効な場合、あるいは合併症(出血、穿孔、胆汁逆流など)がある場合には、手術が検討されます。
以下は当院で経験されたピロリ陽性例での二重幽門の症例です。
(1)Wiseman SM, Tan D, Hill HC. Double pylorus: an unusual endoscopic finding. Endoscopy. 2005;37:277. [RCA] [PubMed] [DOI] [Full Text] Lei JJ, Zhou L, Liu Q, Xu CF. Acquired double pylorus: Clinical and endoscopic characteristics and four-year follow-up observations. World J Gastroenterol 2016; 22(6): 2153-2158 [PMID: 26877621 DOI: 10.3748/wjg.v22.i6.2153]
(2)Wolters VM, Nikkels PG, Van Der Zee DC, Kramer PP, De Schryver JE, Reijnen IG, Houwen RH. A gastric diverticulum containing pancreatic tissue and presenting as congenital double pylorus: case report and review of the literature. J Pediatr Gastroenterol Nutr. 2001;33:89-91. Lei JJ, Zhou L, Liu Q, Xu CF. Acquired double pylorus: Clinical and endoscopic characteristics and four-year follow-up observations. World J Gastroenterol 2016; 22(6): 2153-2158 [PMID: 26877621 DOI: 10.3748/wjg.v22.i6.2153]
(3)Hu TH, Tai DI, Changchien CS, Chen TY, Chang WC. Double pylorus: report of a longitudinal follow-up in two refractory cases with underlying diseases. Am J Gastroenterol. 1995;90:815-818. [PubMed] [DOI]
(4) Fattahi MR, Homayoon K, Hamidpour L. Double pylorus in a cirrhotic patient: a case report and review of the literature. Middle East J Dig Dis. 2012;4:130-132. [PubMed] 18. Costa S, Dias VC, Peixoto P, Machado A, Gonçalves R. Double pylorus. Rev Esp Enferm Dig. 2015;107:377. [PubMed]
(5)Lei JJ, Zhou L, Liu Q, Xu CF. Acquired double pylorus: Clinical and endoscopic characteristics and four-year follow-up observations. World J Gastroenterol 2016; 22(6): 2153-2158 [PMID: 26877621 DOI: 10.3748/wjg.v22.i6.2153]
文責 院長 岡田和久
胃悪性リンパ腫(ピロリ陰性)⑤(胃カメラ/胃内視鏡)
MALTリンパ腫はリンパ濾胞のmarginal zoneからのmucosa-associated lymphoid tissu由来であり、B細胞リンパ腫の一種です。
さまざまな肉眼的形態を示し、早期胃癌類似型、胃炎類似型、隆起型などに大別されますが(1)、
本例のような陥凹限局型の胃MALTでは、内視鏡的に未分化型の早期癌との鑑別が問題になります。
H.pylori感染が認められる場合には除菌治療が第一選択となり、80%程度が完全寛解しますが、除菌治療が奏功しない場合やH.pylori未感染の場合には、
限局期(stageIないしIIa)であれば低線量放射線治療が有効です(2)。
他方でH.pylori未感染であっても除菌治療が有用な例が報告されており、その中にはH.heilmanniiなどのNHPHが関与している可能性を考慮する必要があります(4)。
本例ではH.pylori未感染に発生した3-4mm大の退色調の陥凹性病変で、生検でMALTの診断となり、放射線治療が施行されました。
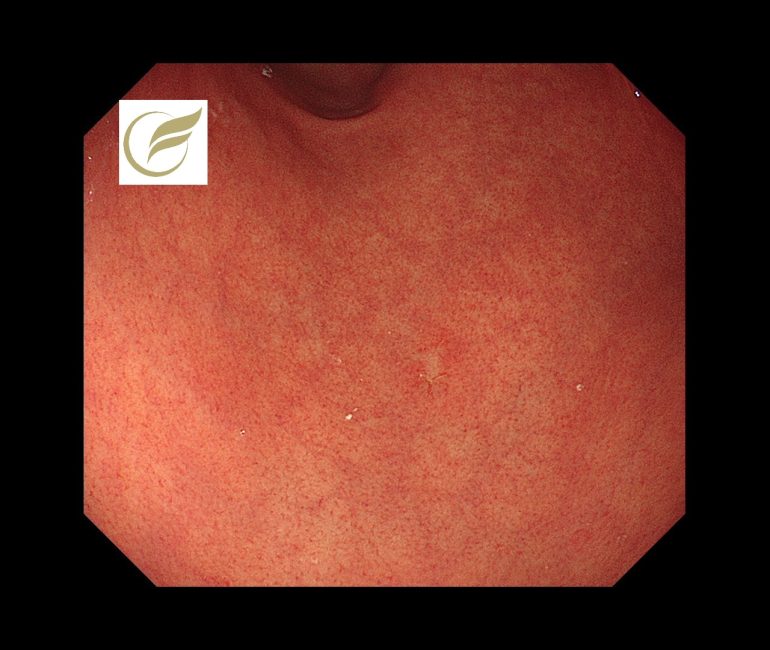
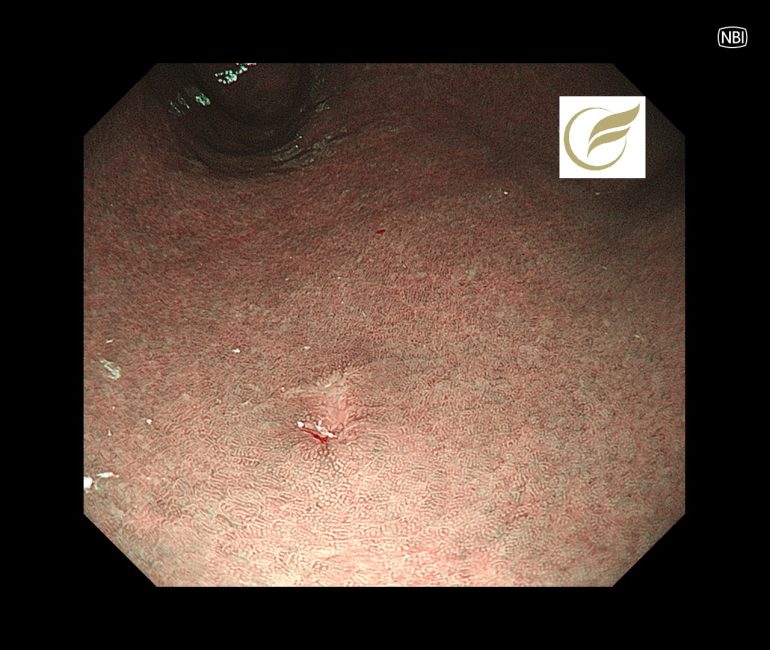
参考症例①
Comparison of localized gastric mucosa-associated lymphoid tissue (MALT) lymphoma with and without Helicobacter pylori infection
Taiji Akamatsu et al. PMID: 16579838
Long-term clinical outcome of gastric MALT lymphoma after eradication of Helicobacter pylori: a multicentre cohort follow-up study of 420 patients in Japan
Shotaro Nakamura et al. PMID: 21890816 DOI: 10.1136/
十二指腸GIST③(胃内視鏡/胃カメラ)
GISTは中胚葉由来の消化管間葉系腫瘍であり、消化管固有筋層にあるCajal介在細胞(消化管内の食物を運ぶ働きに関係している神経細胞)から発生した腫瘍と考えられています。
小さいうちには症状はなく、検査で偶発的に見つかることが多いのですが、増大にしたがって出血、腹痛、腫瘤蝕知などを認め、発見にいたることもあります。
GISTの好発部位は胃が60%、小腸が30%、大腸5%、食道5%といわれており、十二指腸は全体の3-5%とされています(1-4)。
十二指腸のうち、下行部、水平部・上行部・球部の順に多いとの報告もあります。
GISTは悪性化する潜在性がある腫瘍であり、GIST診療ガイドラインで、治療の第一選択は基本的に外科切除とされています(5)。
以下は当院で経験された十二指腸下行脚の十二指腸GISTです。症状はありませんでした。
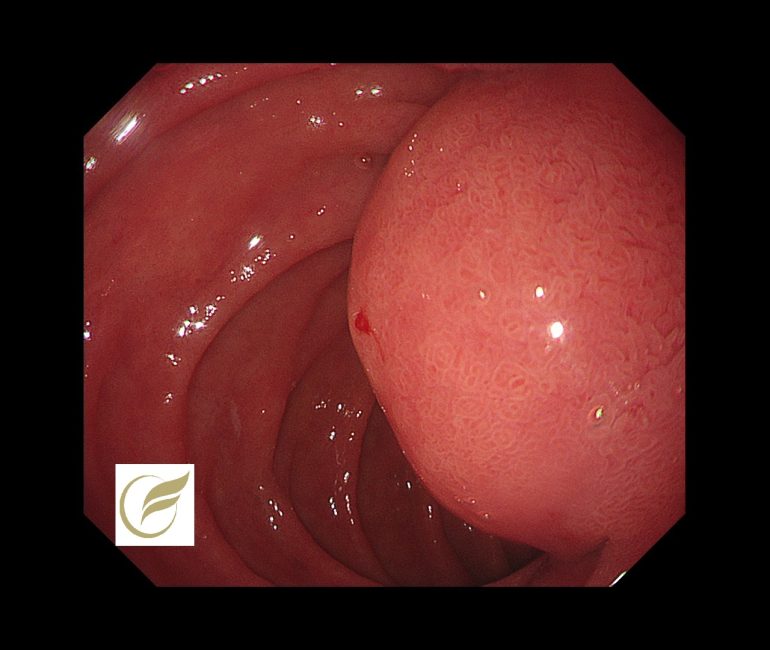
参考症例
参考文献
(1)消化器内視鏡Vol35 No4 2024 P522-523
(2)臨床と研究96 P843-847 2019
(3)臨床外科74 P889-892 2019
(4)Gastrointestinal stromal tumors: pathology and prognosis at different sites.
(5)日本癌治療学会 GIST診療ガイドライン 2022年4月改定第4版 http://www.jsco-cpg.jp/gist/
文責 院長 岡田和久
胃特発性潰瘍② (胃内視鏡/胃カメラ)
本邦において、特発性潰瘍(IPU) の罹患率が増加している可能性が示唆されています(1、2)。
IPUの危険因子ははっきりしていませんが、潰瘍の発生部位はH. pylori 陽性潰瘍と比較して、前庭部から十二指腸球部に多く認められ、
単純な H. pylori 陽性潰瘍と比較して難治性で再発率が高いことが報告されており、
特に 萎縮性胃炎がなく除菌歴のない患者では、治癒率がより低く、再発が多く認められるとの報告もあります(3)。
難治性であっても最終的に瘢痕化が得られる症例がほとんどですが、日常診療においてもPPIの減量や中止で再発することが多く経験され、
報告においてもIPUと出血性 H. pylori 潰瘍では、IPU 群において累積再発率、出血率、総死亡率が高いと報告されており、
酸分泌抑制薬投与による再発防止と厳重な経過観察が必要とされています。
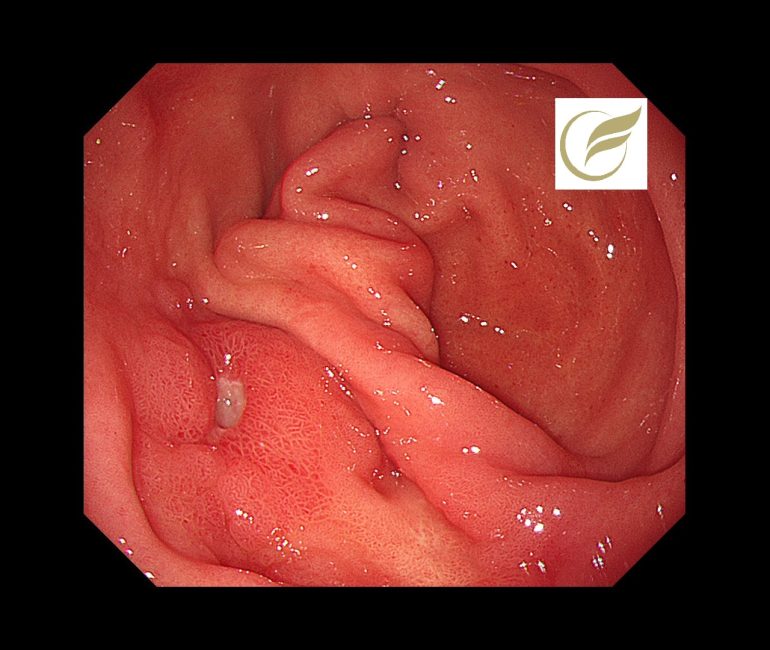
参考文献
消化器内視鏡Vol.34 増刊号2024 P188-189
日消誌 2023;120:816―826
(1)J Gastroenterol Hepatol. 2015 May;30(5):842-8. doi: 10.1111/jgh.12876.PMID: 25532720
(2)J Gastroenterol. 2019 Nov;54(11):963-971.
(3)Dig Endosc. 2016 Jul;28(5):556-63. doi: 10.1111/den.12635. Epub 2016 Apr 3
文責 院長 岡田和久
胃特発性潰瘍①(胃内視鏡/胃カメラ)
消化性潰瘍の二大要因は、Helicobacter pylori(H. pylori)と非ステロイド性抗炎症薬(NSAIDs)ですが、これらを要因としない原因不明の消化性潰瘍は、特発性潰瘍(idiopathic peptic ulcer disease;IPU)とよばれます。
明確な成因は不明ですが、単純な H. pylori 陽性潰瘍と比して基礎疾患の合併が多いこと、難治で再発率が高いことが指摘されています。
近年 H. pylori の除菌が進むにつれ,消化性潰瘍における IPU の割合が増加しています。
以下は当院で経験されたIPUの一例です。Helicobacter pylori陰性、薬剤処方歴がない症例でした。
参考文献
日消誌 2023;120:816―826
消化器内視鏡Vol.34 増刊号2024 P188-189
文責 院長 岡田和久
食道胃接合部癌④(胃カメラ/胃内視鏡)
食道胃接合部・胃噴門部腺癌は、萎縮性胃炎を背景として発生する場合と酸逆流に関連して発生する場合がありますが、
手術数の増加が報告されており、日本ではHp感染率の低下と、食生活の欧米化などが原因として想定され、今後も酸関連疾患として増加することが予想されています(1、2)。
この領域では、胃の他領域に比較して進行がんで発見される割合が多いのが特徴で、内視鏡的な早期診断が容易でないという点に加え、生物学的に悪性度が高い可能性が示唆されています(3)。
以下は当院で経験された胃食道接合部癌(Type4)です。
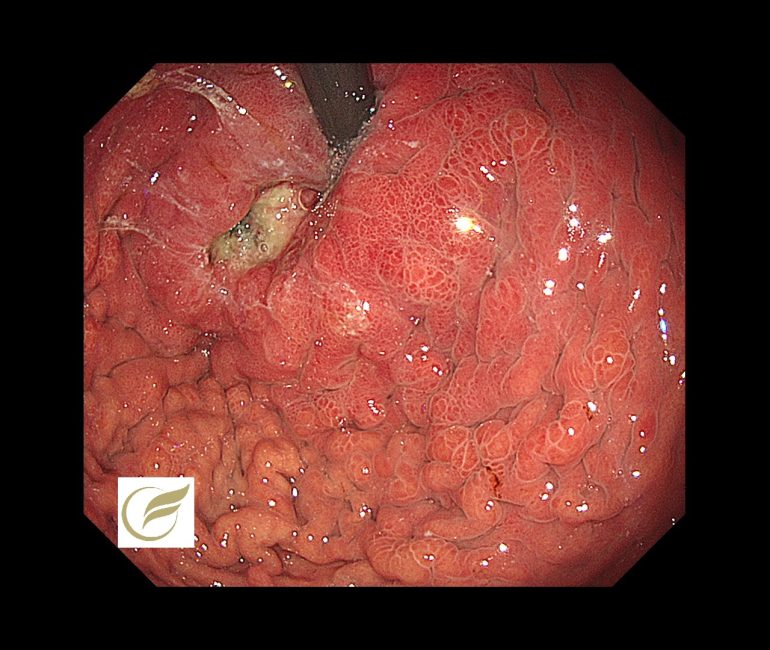
参考文献
(1)Time Trends in Helicobacter pylori Infection and Atrophic Gastritis Over 40 Years in Japan. Helicobacter. 2015 Jun;20(3):192-8. doi: 10.1111/hel.12193. Epub 2015 Jan 7.PMID: 25581708
(2)消化器内視鏡Vol34. No2. 2022 P266-273
Yoshimura D et al.al. Gastric cancer without Helicobactor pylori infection other than gastric cardia cancer is less invasive. Gastroenterology 154:S936, 2018
文責 監修 院長 岡田和久
食道胃接合部癌③(胃カメラ/胃内視鏡)
接合部癌は、早期がんでは症状はありませんが、進行するとつまり感や、貧血などの症状がでる場合があります。
以下も、当院で経験された接合部の進行がんの一例です。
進行がんでは、外科的手術、抗がん剤治療などの治療選択肢があります。
文責 監修 院長 岡田和久